Diamant
Diamant
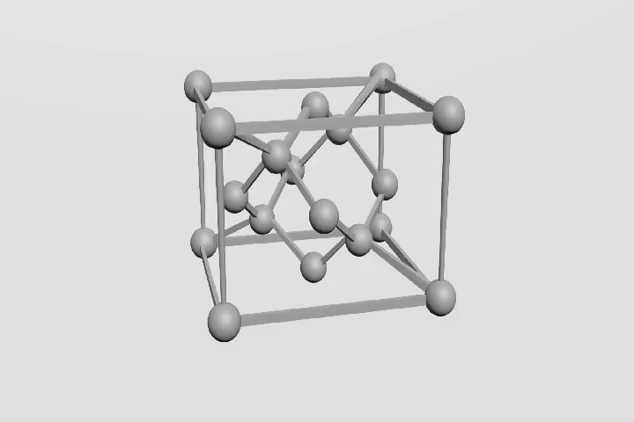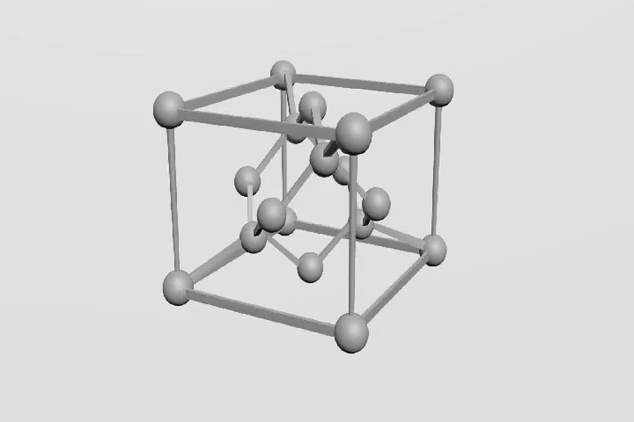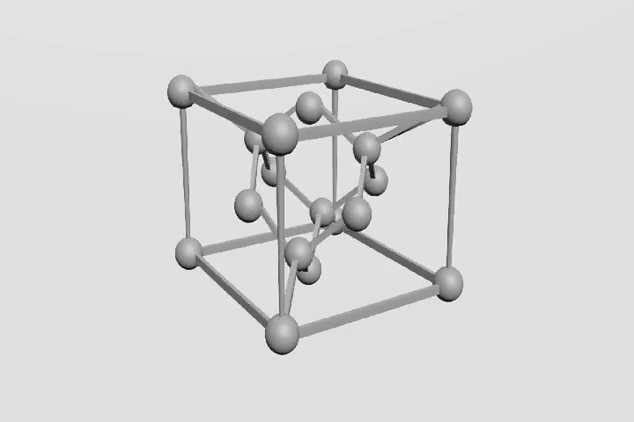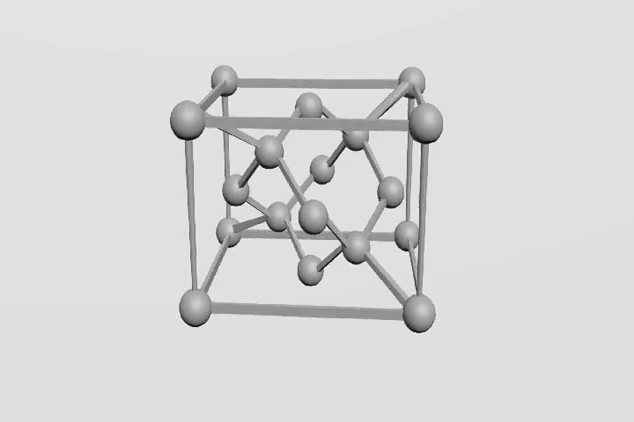
Každý atom uhlíku je poután se čtyřmi sousedními atomy, které jsou umístěny ve vrcholech tetraedru (čtyřstěnu). Vazby mezi uhlíkovými atomy jsou velmi pevné.
je tvořen uhlíkem krystalizujícím v soustavě krychlové a je nejtvrdšíma velmi cenným přírodním nerostem. Na každý uhlík jsou kovalentně vázány další čtyři uhlíky (hybridizace sp3).
Na obrázku Diamanty

Hmotnost diamantů se udává v karátech, největším doposud nalezeným diamantem byl Cullinan, který v surovém stavu při nálezu v JAR dosáhl váhy 3 106 karátů (621,2 gramů). Diamanty se používají pro svou tvrdost a výbornou tepelnou vodivost (až 2300 W•m−1•K−1 při pokojové teplotě a normálním izotopickém složení) v nejrůznějších řezných a vrtných nástrojích. Pro vysokou cenu bývají diamanty vyráběny synteticky.
Přírodní diamanty slouží již od pradávna především k výrobě těch nejdražších šperků. Aby se mohl diamant zasadit do zlatého nebo platinového šperku, musí být nejprve složitě a pečlivě broušen. K úspěšnému vybroušení drahého a vzácného diamantu je třeba nejen značné zkušenosti, ale i zručnosti a trpělivosti. Středisky broušení diamantů a obchodu s nimi jsou belgické Antverpy a nizozemský Rotterdam a Amsterodam.
Na obrázku chemická struktura Diamantu